상단영역
본문영역
전체기사 목록
기사목록 보기 형태
-

-

-

-

-

-

-
 제약/바이오
제약/바이오제약업계, 적자에도 R&D 투자 늘린 곳 어디?
-
-
 이코노미 +
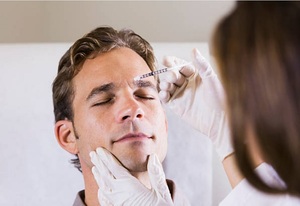
이코노미 +대웅제약, 해외시장 공략 강화 ‘잰걸음’
-

-

-

-

-
-

-
-
-

-

-

