상단영역
본문영역
전체기사 목록
기사목록 보기 형태
-

-
-

-

-

-

-
-

-
 이코노미 +
이코노미 +식약처, 허위·조작 ‘메디톡신’ 퇴출 철퇴
-

-
 이코노미 +
이코노미 +메디톡스, 식약처 상대 ‘발끈’한 이유
-

-
 이코노미 +
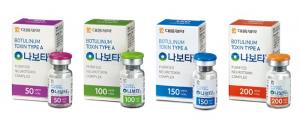
이코노미 +대웅제약, 보툴리눔 톡신 제제 ‘나보타’ 판로 확대
-
 이코노미 +
이코노미 +메디톡스, ‘품질부적합 보톡스’ 수출 가능했던 이유
-

-

-

-
 이코노미 +
이코노미 +‘사면초가’ 메디톡스, 깊어지는 주름살
-
 이코노미 +
이코노미 +상장제약사 영업이익률 9.8%… 바이오 업체 강세
