상단영역
본문영역
전체기사 목록
기사목록 보기 형태
-

-
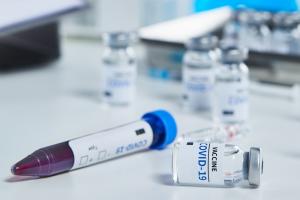
-
-

-
-
 이코노미 +
이코노미 +아스트라제네카 백신 도입, 차질 없을까
-

-

-
 이코노미 +
이코노미 +유럽서 희귀의약품 지정된 한미약품 항암제 ‘오락솔’
-

