상단영역
본문영역
전체기사 목록
기사목록 보기 형태
-

-
-
-
-
 이코노미 +
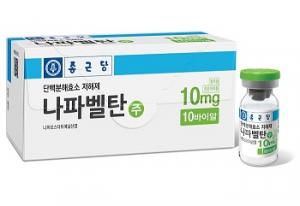
이코노미 +헬릭스미스, ‘엔젠시스’ 상용 생산 파트너 확보
-

-

-

-

-

-

-
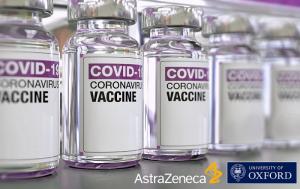 이코노미 +
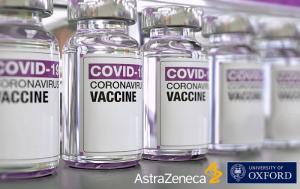
이코노미 +아스트라제네카 백신 도입, 차질 없을까
-
-
-

-
 이코노미 +
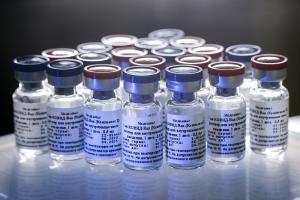
이코노미 +글로벌 제약사, 코로나19 백신 개발 레이스 치열
-

-

-

-

