IBS 연구진, 별세포 단백질 ‘SIRT2’의 기억력 상실 원리 규명

시사위크=박설민 기자 국내 연구진이 알츠하이머 치매의 기억력 저하에 관여하는 뇌 속 단백질을 새롭게 규명하는데 성공했다. 알츠하이머의 신규 치료 및 예방 연구에 큰 보탬이 될 것으로 기대된다.
기초과학연구원(IBS)은 이창준 인지 및 사회성 연구단 단장과 므리둘라 발라(Mridula Bhalla) 박사후연구원 연구팀이 뇌 속 별세포가 발현하는 단백질이 기억력 손상 유발의 핵심 기전임을 증명했다고 14일 밝혔다. 연구팀은 또한 이 단백질을 억제해 단기 기억력 회복이 가능하다는 사실도 증명했다.
‘알츠하이머(Alzheimer’s)’는 베타 아밀로이드 단백질이 뇌의 신경세포를 손상시켜 발생하는 뇌질환이다. 치매 발병 원인 중 가장 많은 비율을 차지한다. 서울아산병원에 따르면 전체 치매의 50~60%가 알츠하이머에 의한 것이다. 특히 알츠하이머의 가장 치명적인 증상은 기억력 상실이다. 하지만 아직까지 뚜렷한 원인이 밝혀지지 않아 치료법 개발에 난항을 겪고 있다.
이에 IBS 연구진은 알츠하이머로 인한 기억력 상실의 원인을 상세히 규명하는 실험을 진행했다. 그 결과, 뇌 속 별세포가 발현하는 단백질 ‘시트루인2(SIRT2)’가 기억력 손상을 유발하는 신경전달물질의 생성을 조절하는 핵심 단백질임을 밝혀냈다.
‘별세포(astrocyte)’는 별모양의 비신경 뇌세포다. 전체 뇌세포의 절반 이상을 차지한다. 신경세포 간 신호전달을 조율하고 뇌 기능을 안정적으로 유지하는 역할을 한다. 알츠하이머나 뇌 염증과 같은 질병 환경에서는 별세포의 수와 크기가 증가한다.
이때 알츠하이머에 걸린 뇌의 별세포들은 ‘반응성 별세포(reactive astrocyte)’로 변한다. 이로 인해 질병 초기부터 염증 반응을 유도하고 신경 퇴행의 시작과 진행에 깊게 관여하는 것으로 알려져 있다.
연구진은 별세포가 발현하는 단백질인 SIRT2에 주목했다. SIRT2는 ‘가바(GABA)’ 생성을 조절하는데 중요한 관여를 하기 때문이다. 여기서 가바란 억제성 신경전달물질이다. 알츠하이머로 인해 가바가 과도하게 발생할 경우 뇌의 신호전달이 억제돼 기억력 감퇴가 유발될 수 있다.
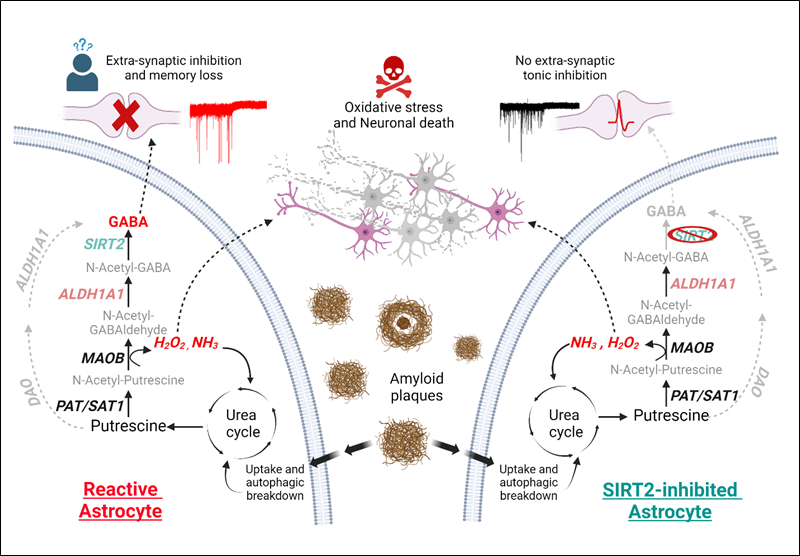
이에 연구진은 알츠하이머 모델 생쥐의 별세포에 발현되는 유전자들을 분석했다. 그 결과, SIRT2의 발현이 비정상적으로 증가해 있음을 확인했다. 이에 별세포에서 SIRT2를 유전자 수준에서 억제하거나 약물을 처리해 활성을 억제하는 실험을 진행했다.
실험용 쥐의 별세포의 SIRT2를 억제한 결과, 별세포 내 가바 생성이 절반 가까이 감소했다. 신경세포에 대한 억제 작용도 약 30~40% 줄었다. 또한, SIRT2 억제가 실제 기억력 회복으로 이어지는지 확인하기 위한 실험 생쥐 미로 실험도 진행했다. 그 결과, 손상된 단기 기억이 정상 수준 가까이 회복되는 효과를 보였다.
연구진은 또 다른 단백질 ‘알데히드 탈수소효소 1A1(ALDH1A1)’의 역할도 함께 확인했다. SIRT2가 가바 생성을 결정짓는 핵심 효소임을 명확히 확인하기 위함이다. 실험 결과 ALDH1A1을 억제했을 때도 가바 생성이 감소했다. 하지만 SIRT2를 억제했을 때만큼 완전히 차단되지는 않았다.
므리둘라 발라 박사후연구원은 “현재 알츠하이머 치료에 사용되는 MAO-B 억제제는 가바와 신경 세포 유발 과산화수소를 광범위하게 억제한다”며 “이번 연구는 가바와 과산화수소가 각각 치매에 어떤 영향을 미치는지 심층 연구할 수 있는 중요한 단서를 확보한 것”이라고 설명했다.
이창준 IBS 단장은 “이번 연구는 별세포의 대사 경로를 조절해 알츠하이머 치매의 기억력 저하를 완화할 수 있는 가능성을 제시했다”며 “특히 SIRT2는 가바 생성을 선택적으로 조절하는 핵심 표적으로 정밀한 치매 치료제 개발을 위한 유효 타깃이 되길 기대한다”라고 밝혔다.
이번 연구 성과는 국제 학술지 ‘몰레큘러 뉴로디제너레이션(Molecular Neurodegeneration, IF 14.9)’에 지난 1월자로 온라인 게재됐다.

